Уважаеми медицински специалисти,
Novo Nordisk A/S и в частност Ново Нордиск Фарма ЕАД, съгласувано с Европейската агенция по лекарствата и Изпълнителната агенция по лекарствата (ИАЛ), бихме искали да Ви информираме за следното:
Резюме
- Таблетките Rybelsus® ще бъдат заменени с нов състав с повишена бионаличност, който е биоеквивалентен на първоначалния състав, както е описано в таблицата по-долу:
|
Първоначален състав |
Биоеквивалентност |
Нов състав |
|
3 mg (начална доза) |
= |
1,5 mg (начална доза) |
|
7 mg (поддържаща доза) |
= |
4 mg (поддържаща доза) |
|
14 mg (поддържаща доза) |
= |
9 mg (поддържаща доза) |
- Новият състав има същата ефикасност, безопасност и начин на приложение като първоначалния.
- Приемът на Rybelsus® винаги трябва да бъде по една таблетка на ден.
- За известен период двата състава ще бъдат налични съвместно на пазара, което може да доведе до объркване. Това може да доведе до предозиране, което увеличава риска от нежелани събития.
- Пациентите, които в момента приемат Rybelsus®, трябва да бъдат информирани и съветвани относно промяната в състава и дозата, в момента на предписване или на отпускане на новия състав.
- На пациентите, които започват лечение с Rybelsus®, трябва да се предпише новия състав и да бъдат подходящо информирани от предписващия лекар или фармацевта.
Причини за опасенията, свързани с безопасността
Rybelsus® е с индикация за лечение на възрастни с незадоволително контролиран захарен диабет тип 2 като допълнение към диета и физически упражнения.
Novo Nordisk заменя първоначалния състав (таблетки от 3 mg, 7 mg, 14 mg) на Rybelsus® с новия състав (таблетки от 1,5 mg, 4 mg, 9 mg).
В сравнение с първоначалния състав, ексципиентите в новия състав са модифицирани, за да се увеличи абсорбцията. Новият състав има повишена бионаличност, което води до по-ниски дози за постигане на същата лекарствена експозиция. Биоеквивалентността е демонстрирана в клинично изпитване и дозите на новия състав имат същата ефикасност и безопасност като първоначалния състав. Това означава, че данните генерирани във фаза 3 на програмата за клинично изпитване на Rybelsus®, са приложими за новия състав. Това позволява преминаване между съответните дози от първоначалния състав и новия състав. Начинът на приложение остава същият.
Съвместното съществуване на двата състава по време на преходния период може потенциално да доведе до объркване и да създаде риск от лекарствени грешки. Лекарствените грешки могат да доведат до повишена експозиция на семаглутид, което може да доведе до стомашно-чревни нежелани събития, напр. гадене, повръщане и диария.
Продуктовата информация е актуализирана, за да обясни разликата между двата състава и да даде възможност на читателите да идентифицират еквивалентните дози в съставите с биоеквивалентни дози.
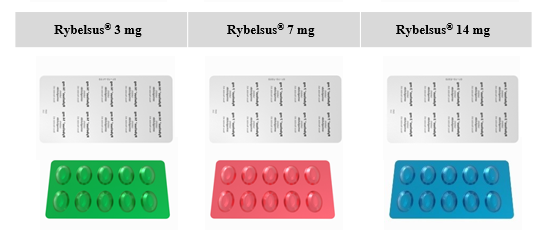
Опаковката и формата на таблетката за новия състав се различават от първоначалния състав, но цветът на различните стъпки на дозиране е запазен подобен. Вижте таблицата по-долу.
|
Размер на таблетката: Таблетките на новия състав са с по-малък размер и различна форма (кръгли). Таблетките са с вдлъбнато релефно означение на концентрацията. |
Първоначален | Нов
|
|
Първична опаковка: Блистерите на новия състав са сребристи както отпред, така и отзад и са по-малки в сравнение с блистерите на първоначалния състав. |
Първоначален състав
Нов състав
|
|
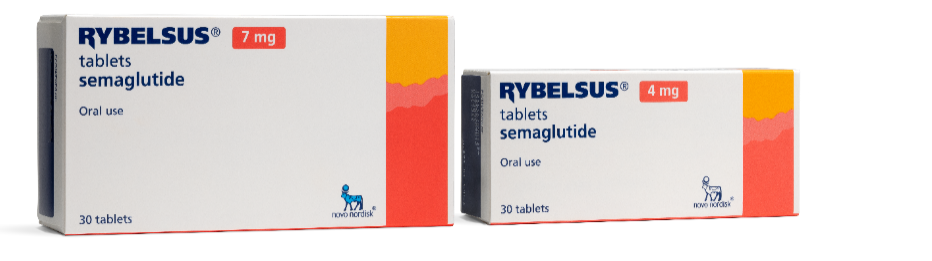
Вторична опаковка: Картонените кутии на новия състав са по-малки |
Картонена кутия на първоначален състав | Картонена кутия на нов състав
|
Призив за съобщаване на нежелани лекарствени реакции
Бихме искали да напомним, че медицинските специалисти са задължени според Закона за лекарствените продукти в хуманната медицина (ЗЛПХМ) да съобщават незабавно на притежателя на разрешението за употреба или на Изпълнителна агенция по лекарствата (ИАЛ) за всяка подозирана сериозна нежелана лекарствена реакция и да предоставят при поискване допълнителна информация от проследяването на случая.
Притежател на разрешението за употреба/Представител на ПРУ
Ново Нордиск Фарма ЕАД
бул. „Черни връх“ № 51, Бизнес Гардън Офис X, сграда 3, етаж 4
гр. София 1407
тел: 02/ 962 74 71
mail: Този имейл адрес е защитен от спам ботове. Трябва да имате пусната JavaScript поддръжка, за да го видите.
Изпълнителна агенция по лекарствата (ИАЛ)
ул. Дамян Груев № 8
1303, гр. София
Р. България
тел.: +359 2 8903 417
факс: +359 2 8903 434
e-mail: Този имейл адрес е защитен от спам ботове. Трябва да имате пусната JavaScript поддръжка, за да го видите.
Формуляр за съобщаване на нежелани лекарствени реакции от медицински специалисти
Съобщавайте нежеланите реакции на Изпълнителна агенция по лекарствата:
- тел.: +359 2 8903417
- e-mail: Този имейл адрес е защитен от спам ботове. Трябва да имате пусната JavaScript поддръжка, за да го видите.
Онлайн:
 Формуляр за съобщаване на нежелани лекарствени реакции от медицински специалисти
Формуляр за съобщаване на нежелани лекарствени реакции от медицински специалисти